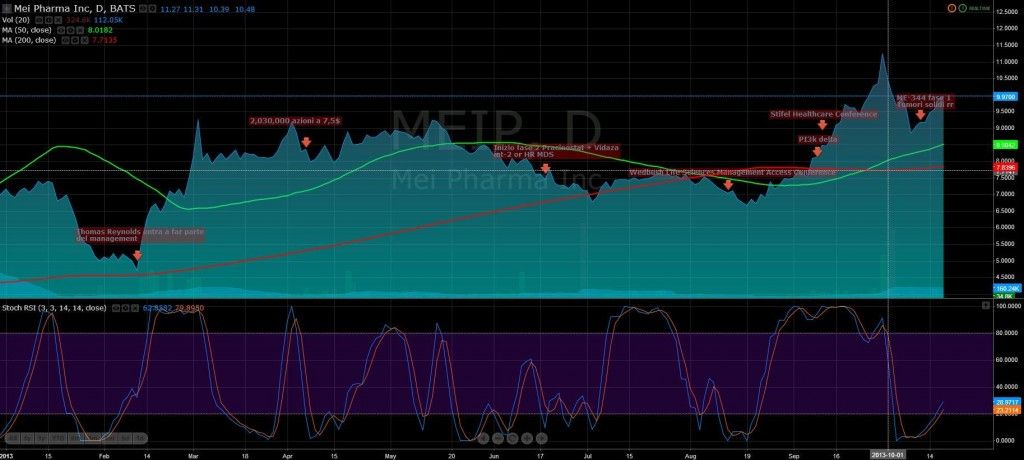
Di MEI Pharma ho parlato lo scorso aprile, dopo che la compagnia aveva provveduto a finanziarsi emettendo nuove azioni. In quel periodo il titolo quotava attorno agli 8 dollari, oggi si trova, a sei mesi di distanza, a quota 10$. Considerando che l’offerta di azioni è stata fatta ad un prezzo scontato attorno ai 7 dollari è interessante notare che il titolo non è quasi mai sceso sotto tale soglia. Vi riporto un grafico con alcuni degli eventi più importanti accaduti nel corso del 2013:
Pracinostat, HDAC inibitore e farmaco in fase più avanzata della compagnia, è entrato in fase 2 a giugno. Lo studio è randomizzato vs placebo e vede il composto impiegato in combinazione con Vidaza su pazienti affetti da sindromi mielodisplastiche in prima linea. Un ulteriore fase 2 è in procinto di iniziare a breve ma riguarderà pazienti in età avanzata, affetti da leucemia acuta linfoblastica (AML) e non candidabili per terapie di induzione. Pracinostat però non è il farmaco più interessante di MEI Pharma. Pur potendo consentire all’azienda di tentare la strada per un’approvazione in tempi relativamente brevi, il valore di MEI Pharma è nel programma relativo al metabolismo del cancro, programma che vede interessati i farmaci ME 143 e ME 344. Completa la pipeline il recente acquisto di PWT 143, PI3k delta inibitore sviluppato originariamente da Pathway Therapeutics.
Pochi giorni fa MEI Pharma ha anticipato quelli che saranno i dati discussi con dovizia di particolari il 20 ottobre al meeting AACR-NCI-EORTC. Per il momento sappiamo che in fase 1 su soggetti affetti da tumori solidi refrattari ai precedenti trattamenti ME 344 ha permesso di ottenere un tasso di controllo della malattia del 35%. Su 23 pazienti valutabili MEI Pharma ha ottenuto una risposta parziale (PR) in un sogetto con tumore al polmone a piccole cellule refrattario (rSCLC) e 7 stabilizzazioni della malattia da un minimo di 8 ad un massimo di 40 settimane. Nel corso dello studio è stata stabilita la massima dose tollerata in 10 mg/kg per un trattamento su base settimanale mentre a dosaggi maggiori (15 e 20 mg/kg) si sono osservati casi di neuropatia periferica (PN) di grado 3. Sebbene il fatto che di tre dosaggi sia solo quello inferiore a venir tollerato senza gravi complicazioni, va detto che l’evento avverso è comune a farmaci con simile meccanismo d’azione. Non è un dramma nel contesto dello studio, potrebbe risultare problematico a seconda del tipo di trattamento somministrato in combinazione con ME 344.
Sul versante dell’efficacia è interessante la PR nel paziente con tumore al polmone a piccole cellule (SCLC) anche in considerazione della durata della risposta (oltre un anno), ma è troppo poco per trarre delle conclusioni. Domenica potrebbero arrivare nuove ed importanti informazioni, considerando che la scadenza per la presentazione dell’abstract all’AACR-NCI-EORTC era a metà agosto. Si può immaginare che saranno forniti aggiornamenti sia sul versante del numero, della qualità e della durata delle risposte, oltre che ad un aggiornamento sulla tollerabilità del farmaco.
L’importanza di questi dati risiede nel fatto che sono praticamente i primi riguardanti farmaci che hanno come obiettivo il metabolismo del tumore. Agios (AGIO) può essere annoverata come una diretta concorrente di MEI Pharma, anche se l’approccio è differente e la recentemente sbarcata sul Nasdaq può vantare già partnership di livello mondiale con Celgene. MEI Pharma dal canto suo si trova in una fase di sviluppo leggermente più avanzata e può trovare una strada tutta sua, a partire (se i dati lo confermeranno) dal SCLC.
Agios per il momento ha iniziato una fase 1 in soggetti affetti da AML e con specifica mutazione IDH2 e capitalizza quasi 900 milioni di dollari, MEI Pharma è quasi pronta per scegliere un’indicazione da portare in fase 2 e capitalizza 170 milioni. Mi pare evidente che ci sia qualcosa che non quadra in tutto questo, o no?

‘mazza oh! già ‘sta MEIP è tutta ‘na discesa, poi n’annetto fa ha pure splittato……
Mo’ che se fa? Se compra MEIP o se lassa stà co’ tutto?
Simo’, sei sempre il solito burlone! 😀
Elisa
Vedo meglio Meip dopo l’emissione piu per un discorso di capitalizz.
CK ovviamente non mi ha influenzato con il suo ultimo post…..
😉