Geron (GERN) è una compagnia che si può descrivere con una sola frase e che più o meno dovrebbe suonare come: “una biotech all’ultima spiaggia”. Se ricordate la Geron di qualche mese fa e la confrontate con quella attuale vi renderete conto del fatto che si tratta di due compagnie diverse e che quella attuale ruota interamente attorno ad un unico farmaco: Imetelstat. Il resto della pipeline è stato inghiottito da un vortice di incompetenza e di scelte che nel settore non pagano come quella di incaponirsi nel segmento delle cellule staminali senza nessun motivo veramente valido, scelta che non ha finora fatto la fortuna di nessuno fra le small cap.
Ora la compagnia si trova nella seguente situazione: non solo quasi tutta la pipeline è stata azzerata ad eccezione di Imetelstat, ma di questo farmaco è stata fermata la sperimentazione nell’ambito dei tumori solidi, lasciando aperto solo lo spiraglio per quanto riguarda il settore ematologico. Capite ora il senso di “ultima spiaggia”?
La buona notizia per Geron è che nei tumori del sangue, i primi segnali di Imetelstat sono molto incoraggianti. La buona notizia per chi volesse investire in Geron è che non molti si sono accorti di questo. L’operazione ce farò oggi è quella di andare a pescare un pezzo da collezione in una stanza piena di chincaglieria. Può succedere di trovarne uno anche se la domanda è sempre la stessa, come può una persona che si è circondata di paccottiglia avere un pezzo di valore fra tanta merce che di valore non ne ha?
Geron ha colpe importanti per come ha gestito la pipeline finora e gli azionisti di lungo corso probabilmente ricorderanno la lunga serie di insuccessi che ha costellato il cammino della compagnia. Ma persino l’azionista più disilluso non può fare a meno di concordare con me su un punto: Geron ha saputo tagliare i rami secchi con una coerenza che non appartiene alla maggior parte di compagnie biotech in circolazione. Gli esempi fateli pure voi, ce n’è a dozzine.
Lo scorso dicembre Geron ha fatto calare la scure su GRN 1005, reo di aver prodotto scarsi risultati e di non riuscire a richiamare l’interesse della comunità medica, il che si è tradotto in un arruolamento lentissimo. Ora, che Geron abbia giustificato il fatto in modo francamente puerile non può offuscare il coraggio nel determinare la fine del progetto.
Come se questo non bastasse, anche metà dell’area di sviluppo di Imetelstat è stata cancellata, visto il mancato raggiungimento degli obiettivi legati alla fase 2 nel tumore al polmone e dal fatto che l’impiego del farmaco in pazienti con tumore al seno HER2 negativo hanno condotto ad una progressione libera da malattia inferiore al braccio di controllo.
Arriviamo quindi al capitolo tumori del sangue. Qui la musica cambia.
Geron, caccia all’allele!
Geron ha riportato i dati di Imetelstat nel trattamento della tombocitemia essenziale (ET da qui in poi, se vi interessa approfondire la malattia, date uno sguardo al box apposito qui sotto, aiuterà a capire alcuni concetti) che, dal mio punto di vista, sono stati trascurati per un motivo sbagliato.
Stando a quanto afferma Geron, Imetelstat è il primo inibitore della telomerasi in fase clinica. La telomerasi è un bersaglio espresso in una moltitudine di tumori, il che renderebbe l’impiego del farmaco giustificato in diverse indicazioni, il che, come ho detto prima, sappiamo non essere vero nel caso di Imetelstat. I telomeri sono i deputati al controllo della duplicazione cellulare, sono piccoli segmenti di DNA posti alla fine del cromosoma e sono balzati agli onori della cronaca quando si è cominciato ad associarli all’invecchiamento, suggerendo l’ipotesi che si potesse agire sull’invecchiamento dell’intero organismo agendo su di essi. Finora è fantascienza, ma l’impiego in ambito terapeutico nel trattare i tumori è una questione piuttosto interessante.
Geron ha illustrato ad ASH 12 i dati già anticipati di Imetelstat in 14 pazienti affetti da ET con le seguenti caratteristiche:

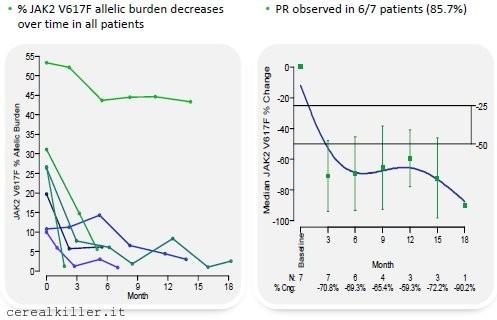
Come vedete, tutti e 14 pazienti avevano ricevuto almeno una linea di trattamento con idrossiurea e la metà di questi si era mostrata resistente ad almeno una terapia. Il dato più interessante però riguarda i pazienti con mutazione del gene JAK2. Se infatti, a livello generale, possiamo dire che tutti e 14 i pazienti hanno ottenuto una risposta ematologica completa (13 su 14 una risposta completa, uno su 14 una parziale), in termini di percentuale di alleli mutati il farmaco promuove una diminuzione nel tempo in tutti e 7 i casi:

Tutto questo condito con un profilo di sicurezza tranquillizzante accompagnato dalla possibilità di ridurre la somministrazione del farmaco in pressoché tutti i pazienti.
Quello che fa passare Geron sotto i radar di molti è il fatto che abbiano scelto di testare il farmaco in una indicazione che molti prima di lei hanno scelto di perseguire solo dopo aver determinato l’efficacia del farmaco in ambiti più remunerativi. Il discorso in questo caso è, e trattandosi di Geron prego tutti di osservare qualche secondo di religioso silenzio, molto più sensato di quanto ci si possa aspettare: iniziare con il trattamento dell’ET era il modo migliore per effettuare una prova di concetto in tempi brevi. Missione riuscita.
Il 13, ossia domani, Geron terrà la conferenza per illustrare i dati economici e lo sviluppo di Imetelstat. Ci aggiorniamo dopo averla seguita.
Salve Francesco, ci sono eccome… l’ultimo articolo riguardo Geron è qui:
http://cerealkiller.it/ash-screener-mielofibrosi/
in linea di massima come altre novità ci sono la partnership di pacritinib fra $CTIC e $BAX e l’imminente inizio di uno studio registrativo che confronterà il farmaco con Jakafi e che molto probabilmente arruolerà anche in Italia, così come sta già facendo l’altra fase 3 di pacritinib, nella quel però il controllo non è costituito da Jakafi.
Sta arruolando anche momelotinib, ma per il momento solo in USA…
tra tutte queste terapie in fase di sperimentazione l’unica che sembra essere efficace nei confronti della malattia è quella con Imetelstat, mentre le altre curano i sintomi più severi, come l’aumento del volume splenico… ma i dati sono ancora prematuri e qualche dubbio circa l’utilizzo in monoterapia permane…
Molto interessante. Ma questo articolo è di Marzo 2013, mi chiedo se ci sono ulteriori notizie in data odierna. Sono interessato perchè ho mia moglie con mielofibrosi in fase avanzata e quindi gradirei essere informato. Grazie