Anche questa edizione di ASH15 va in soffitta e come immaginavo al posto dei fuochi d’artificio finali c’è stata una pioggia di vendite sui mercati. Non è detto che sia finita e non è detto che sia generalizzata, di certo ci sono alcuni aspetti che giustificano, se non pessimismo, l’incrinarsi di una visione estremamente positiva su alcuni temi. Il più evidente, per quanto mi riguarda, è legato all’impiego di terapie CART, con qualche possibile eccezione. Se si possono eleggere vinti e vincitori, fra i primi rientra di certo Idera (IDRA), fra i secondi bluebird bio (BLUE), ma non tutto è semplice come appare.
IDRA
Sapete vita, morte e miracoli di Idera perché avete letto il mio report e ricordate benissimo che avevo indicato un ORR tra il 30 ed il 40% come un buon risultato e quindi il fatto che il tasso di risposta sia stato del 40% e del 50% nella popolazione ITT e nella coorte con il dosaggio massimo rispettivamente giustificano il guadagno fatto segnare nei giorni successivi la comunicazione dei dati, giusto? Più o meno. In realtà tale soglia aveva senso sulla base di quanto annunciato nell’abstract presentato da Idera che parlava di 4 linee terapeutiche precedenti in media per i soggetti arruolati, ma nei dati finali le linee precedenti sono solo due. Un ORR del 50% è inferiore a quanto faccia registrare, ad esempio, ibrutinib, quindi non particolarmente brillante, a mio modo di vedere. Alcuni analisti fanno poi notare che il buon esito di questo studio sulla WM aiuterà ad accelerare l’arruolamento dell’altro trial che vede coinvolto IMO-8400, quello sul trattamento del DLBCL. Io non credo. Penso che la velocità di quello studio sia dettata soprattutto dal fatto che i pazienti, già particolarmente malati, devono essere sottoposti a screening per determinare la positività alla mutazione MYD88 L265P, ed il tempo che questa operazione richiede rischia di rendere un paziente non più eleggibile per far parte del trial a causa dell’aggravarsi della sua salute. Tutto male quindi? Non proprio.
Il primo aspetto positivo che colgo è che il farmaco sembra essere molto ben tollerato e quindi immagino un futuro in terapia di combinazione, ad esempio con rituximab o, perché no, con Imbruvica. Non solo, è così ben tollerato che Idera si aspetta di poterlo impiegare anche in dosaggi superiori a quelli testati. Ora, non è che essere a questo punto ed ancora non sapere a quale dosaggio sia meglio impiegare il tuo farmaco di punta sia un elemento di vanto, ma è pur sempre vero che la svolta in ambito ematologico della compagnia è recente, quindi ci si può anche passare sopra.
Secondo aspetto positivo: la svolta appena citata ha senso, perché dalla carta si è passati a dimostrare in clinica che IMO-8400 ha un potenziale in alcune indicazioni ben precise. Come detto si può discutere sulla magnitudo del tasso di risposta ma è innegabile che l’attività ci sia ed è confortante che questa sia correlata e dipendente dal dosaggio, non frutto di fumo generato dallo scarso numero di pazienti.
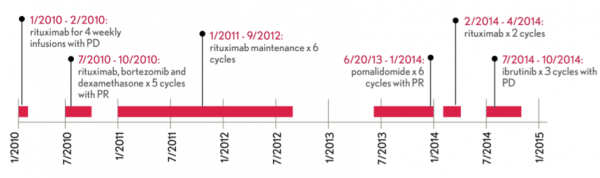
Terzo aspetto positivo, anche se in questo caso è lecito avere più che qualche dubbio, un paziente refrattario ad ibrutinib e che aveva ricevuto 6 linee terapeutiche precedenti ha ottenuto una PR. La sua storia è schematizzata qui sotto:
Conclusione.
Nel portafoglio biotech USA non cambia nulla, la posizione rimane invariata vista la dimostrazione di funzionamento del meccanismo d’azione.
KPTI
Karyopharm ha portato una valanga di materiale ad ASH15 ma credo che i dati più interessanti siano quelli inerenti il trattamento del mieloma multiplo. Non che non ci siano apprezzabili aggiornamenti sul fronte AML, anzi, per quello che ho potuto vedere il profilo di tollerabilità del farmaco è migliore di quanto mi aspettassi e non si vedono segni di ulteriori casi di sepsi, fenomeno che la scorsa estate aveva causato panico fra gli investitori. Selinexor continua ad essere efficace e sembra che chi lo usa stia imparando a farlo nel modo migliore possibile. Questa è una prima notizia importante, ma lo diventa ancor di più se si considera che a breve entrerà in clinica anche il secondo XPO1 inibitore della compagnia: KPT-8602. Già ad ASH15 si è visto qualcosa di interessante, anche se a livello preclinico. Il nuovo arrivato potrebbe essere un selinexor più efficace e più tollerabile e visto l’ampia attività del capostipite è lecito essere ottimisti circa il successore.
Rimanendo alla stretta attualità sono rimasto, come vi accennavo, molto colpito dall’attività di selinexor nel trattamento di soggetti affetti da MM recidivo e refrattario. Un tasso di risposta del 67% in una popolazione molto pretrattata è un risultato eccellente, anche se in pochi pazienti. Sarà importante vedere quanto saranno durature le risposte ma è importante notare che queste si sono verificate molto velocemente e che 5 su 7 pazienti refrattari a carfilzomib hanno ottenuto una PR o una VGPR.
Conclusione
In portafoglio le rimanenti azioni rimangono al loro posto. Il 2016 sarà un anno interessante per Karyopharm, sia per i dati potenzialmente registrativi di selinexor in diverse indicazioni, sia per l’ingresso in clinica del suo follow on.
STML
Stemline ad ASH15 porta dati aggiornati di SL-401 nel trattamento del BPDCN e sono al limite della perfezione: 86% (12/14) ORR nella popolazione ITT con 100% (9/9) ORR in pazienti in prima linea e 60% (3/5) in pazienti recidivi/refrattari. A tutto questi si aggiungono il 57% (8/14) di risposte complete (4CR+ 4CRc), 5 pazienti in remissione e 2 soggetti ai quali è stata garantita la possibilità di arrivare al trapianto. Fare meglio di così è veramente difficile, soprattutto se si considera che 2 delle remissioni sono giunte da pazienti recidivi o refrattari. Difficile capire perché la quotazione sia così bassa a fronte di questi dati, anche ammettendo che Stemlline sia solo questo e niente altro la capitalizzazione di poco più di 100 milioni è senza senso, anche in considerazione del fatto che al 30 settembre in cassa c’erano 104 milioni di dollari.
Conclusione
A fronte dei dati e della quotazione attuale un ingresso in Stemline è decisamente ragionevole con l’ottica di attendere maggiore interesse del mercato verso il programma e gli aggiornamento del 2016. La durata delle risposte sarà l’elemento discriminante per capire quale futuro sarà possibile per la compagnia ed ASCO probabilmente la vetrina più idonea per rendere disponibili questi dati. Al momento il fatto che due pazienti abbiano potuto usufruire del trapianto depone a favore di una durata sufficiente, ma sono necessari maggiori dati.
TGTX
Ero piuttosto curioso di vedere 1303 all’opera ed in particolare di capire come aggiungere 1202 e 1101 ad ibrutinib potesse giovare ai pazienti. Per chi non avesse familiarità con la compagnia o si fosse perso il report su ASH15 potrebbe risultare difficile capire cosa sia 1303 e come mai non figuri un simile farmaco nella pipeline di TG Therapeutics. La risposta è semplice quanto stramba, la compagnia usa quella sigla per indicare la combo TGR-1202 (PI3k inibitore) ed ublituximab (o TG-1101, un anti-CD20). In linea generale gli aspetti più positivi sono che TGR-1202 sembra sufficientemente differenziato rispetto alla concorrenza principalmente grazie al profilo di tollerabilità, mentre dal punto di viste dell’efficacia tutti e due i farmaci continuano a comportarsi in modo egregio. Aggiungere ublituximab ad ibrutinib in pazienti con MCL sembra essere un’ipotesi da tenere in considerazione sulla base del tasso di risposta fatto registrare ed in considerazione di quanto raggiunto da ibrutinib come single agent. In questo caso un’approvazione accelerata sulla base di una fase 2 sarebbe un buon modo per commercializzare il farmaco in tempi ragionevoli, ma qui la concorrenza è più marcata rispetto a 1202, visto il numero considerevole di anti-CD20 (e non solo) in circolazione.
Conclusione
A questi livelli TG Therapeutics è valutata correttamente, secondo me. Passato l’evento binario potrebbe tornare interessante in ottica ASCO. Per il lungo periodo credo che i punti di forza siano la cassa (oltre 100M$), il programma di inibizione IRAK4 e TGR-1202, mentre per le debolezze ublituximab potrebbe non essere così differenziato da avere un futuro roseo, il che potrebbe essere un problema per la combo.
ONTX
Onconova prosegue il suo periodo no durante il quale piazza una fiammata repentina, per poi continuare a sprofondare nell’anonimato. Ad ASH15 portano dati interessanti di Rigosertib che in altri contesti sarebbero stati incoraggianti, sebbene ci siano tutti i limiti dello studio a consigliare prudenza. Nel caso di Onconova però non lasciano il segno perché legati ad un farmaco che ha fallito nel recente passato la sua grande occasione. La compagnia non sembra far molto per invertire il trend e cercare un’alternativa al candidato principale che, se non altro, continua a godere dell’appoggio di Baxter per lo sviluppo in quella particolare indicazione.
Conclusione
La tesi d’investimento in Onconova non cambia, essendo più indirizzata verso un futuro interessante per ON 123300 che per gli sviluppi di rigosertib. Nel breve periodo inoltre medierò la posizione.
AFMD
Affimed porta poco ad ASH15 e quel poco che porta non cambia sostanzialmente la valutazione della compagnia. Il destino nel breve periodo è legato ai dati di AFM11 e quindi rimandato al 2016, quando saranno disponibili i primi dati. Di positivo c’è l’avanzamento del programma anti-CD33, target che ad ASH ha fatto registrare qualche numero di notevole interesse, anche se fornito da altre compagnie.
Conclusione
Sempre long.
BLCM
Due parole veloci su Bellicum. Le terapie basate su CAR-T che si sono viste ad ASH non mi hanno impressionato più di tanto e, in generale, negli ultimi tempi stanno godendo di minore popolarità rispetto a quanto accadesse solo un anno fa. I problemi che ho elencato nel report su ASH15, il fatto che l’efficacia sia al momento praticamente limitata ad alcune forme di leucemia e principalmente in terapie di salvataggio hanno raffreddato molto dell’entusiasmo che permeava queste terapie e le quotazioni delle società che le sviluppavano. Se si esclude il caso Cellectis del quale vi ho parlato, ma che sostanzialmente è più un fenomeno mediatico che abbiamo sfruttato molto bene dal punto di vista dell’investimento, poche tracce rimangono in questa edizione di ASH15 di queste innovative terapie.
Tre sono gli ostacoli più ardui da superare:
- Tollerabilità della terapia
- Scalabilità ed efficienza del processo produttivo
- Efficacia in indicazioni differenti (e più remunerative)
Sebbene Kite stia facendo passi in avanti notevoli se non altro in termini di differenziazione delle indicazioni perseguibili, trovare una compagnia che riesca a sciogliere questi tre nodi gordiani non è semplice. Chiaramente Novartis ha i mezzi per farcela, ma qualora altri big volessero affrontare il problema, non necessariamente sarebbero attrezzati per poterlo fare sfruttando solo strutture interne. Potrebbero aver bisogno di un partner. Detto di Cellectis e del suo approccio allogenico e detto che questo sta riscuotendo un certo successo, al punto da spingere altre compagnie a perseguire la stessa strada, non sono molte le alternative che mi vengono in mente fra le small e medium cap. Una possibilità è Ziopharm (ZIOP) con la sua Sleeping Beauty, che però al momento sembra più addormentata che bella. Un’alternativa possibile è anche Bellicum, che offrirebbe un numero di opzioni decisamente interessante ad un partner di livello. Ad ASH15 il centro dell’attenzione è stata la presentazione dei dati di BPX-501 impiegato in pazienti sottoposti a trapianto di cellule staminali da donatori non perfettamente compatibili (se la cosa vi sembra familiare siete azionisti Molmed). Lo studio presentato ad ASH15 riguardava soggetti pediatrici affetti da diverse malattie e tumori del sangue e sostanzialmente ruota attorno all’ingegnerizzazione dei linfociti T presi dalle cellule dei donatori in modo da aggiungere un interruttore che possa arrestarli in caso di reazioni indesiderate nel paziente che le riceve. Non è tanto il fatto che i dati siano positivi rispetto ai controlli con lo storico, perché come nel caso di Molmed il mercato è di nicchia, quindi non impatta molto sulla valutazione della compagnia, però è rilevante in quanto il meccanismo di sicurezza (chiamato Caspacide) viene applicato da Bellicum sia ai propri CART che ai TCR. Bellicum potrebbe quindi superare tutti e tre gli ostacoli che ho elencato in precedenza, qualora qualche big decidesse di concedere loro fiducia. E soldi.
Conclusione
Bellicum rappresenta un’opzione di investimento molto interessante grazie ad una pipeline molto differenziata ed a una capitalizzazione relativamente bassa. Nel 2016 diversi programmi entreranno in clinica, quindi potrebbe esserci un vuoto dal punto di vista degli eventi nel breve periodo ma la possibilità che un partner si faccia avanti e la cassa che ammontava al 30 settembre a 163 milioni sono motivi sufficienti per una prima posizione.

@Paolo, la prossima volta chiedimi anche i numeri del lotto!
@CK grazie!! dopo averti sognato il 15 per superstizione ho preso TLOG purtroppo solo 500 pz oggi + 35% Auguri
@Celiac & Francesca… sto giusto ora scrivendo due righe per fare gli auguri a tutti e per dire che non so se riuscirò a rifilarvi il pDF per Natale… ma ci provo comunque!
E’…si…un ottimo articolo-post….per Natale ci vuole…….. e se son d’accordo tutti (chi ti segue) con qualche dritta per chiudere l’ anno in bellezza. Mi associo volentieri a Celiakiller un post ci vuole.!!!!
Grazie di tutto…
Buona giornata…
ciao C,K.
Ce lo fai un articolino da leggere sotto l’albero?
BACI
@KarM, molto più probabilmente c’è poco interesse sul titolo ora e magari qualche fondo dopo ASH si è riposizionato altrove. Come detto velocemente nell’ultimo articolo i dati di rigosertib a mio avviso possono essere considerati “incoraggianti”, ma la storia insegna che bisogna essere cauti quando si ha a che fare con certi trials.
Chiedo spiegazioni a che qui dentro e’ poi’ bravo di me (quindi tutti) perche’ davvero non capisco..
ONTX: ma non aveva presentato dei bei dati? com’e’ possibile che ci siano stati picchi a 1.89$, e a distanza di pochi giorni stia soffrendo cosi’ tanto, quotando al momento 1.04$??
E’ tutto fatto per far scattare gli stop loss e far uscire i pesci piccoli?
@Celiac, ecco, appunto! 🙂
C.K.
Io ti metto nel presepe.
@Marco, bene che abbiano centrato l’endpoint… quanto questo valga dal punto di vista clinico è ancora da stabilire.
@Gian, ahahah… se qualcuno deve proprio fare un film su di me, preferisco siano i fratelli Vanzina. Qualcosa tipo “Natale con CK”
@Mikis, su $ARQL hai fatto bene secondo me… $ONTX io credo sia una storia da 2016, non la guarderei molto adesso.
@Juan, che domande… per Natale!
@Celiac, grazie ma mi pare un po’ eccessivo! 😉
@Paolo V, su ARQL si.
CK che ne pensi?
http://seekingalpha.com/pr/15664666-array-biopharma-announces-phase-3-binimetinib-trial-meets-primary-endpoint-for-nras-mutant-melanoma
Ciao CK,hai notato che ormai ti chiamano “Sommo”,”IL Grande”,”Il Verbo”….voci di corridoio a Hollywood dicono che ben presto Spielberg farà un film su di Te intitolato “CK io sono Leggenda! ” 🙂
Ciao grande CK.
Sono riuscito ha leggere tutti i post…tutti i Tuoi report.
Non solo….ho approfondito…e mi ha colpito…la fermezza e l’ approfondimento di cio’ che scrivi…
Veramente interessante.
Ieri grande casiono con Ontx….mannaggia…
Invece di comprare altre azioni ho venduto causa distrazione figli…
Quindi minus…
Poi ho ripreso Ontx…piu’ basse e di piu’….ora andiamo avanti…
Oggi cosa ti aspetti…?
Mi conforti con un discreta risposta?..
Poi…
Primo ingresso Arql…te ne parlavo da tanto…e quindi visto il mercato e il prezzo interessante…ho deciso..
Ciao grazie.
Buona giornata.
@CK per caso sei presente su ARQL e RPTP?
Il VERBO è al lavoro.
mazza ti stai dando da fare ultimamente :-)…fra quanto sara pronto?contando che se dici 2 gg ne passano almeno 4 🙂 son battute ovviamente!!come sempre ti ringrazio!!
@Juan, nel mentre sono al lavoro sul prossimo report…
si vero CK ma CERU è un po un titolo che va per i fatti suoi..cmq per me ieri se FED non fa sorprese domani abbiam visto il bottom
@Paolo V, più probabilmente hai mangiato pesante.
@CK questa notte ho sognato che ti incontravo. Seriamente, ho bisogno di un medico. E pure bravo. Mi ha colpito il fatto che mi parlavi di birinapant. Pensa che non ho letto nulla recentemente. segno premonitore? i cerchi nel grano…??
@Juan, nel mentre piovono coltelli…
CK oggi son entrato anche io nella crew CERU :-)…SPEREMMU!!!
Grazie per il tuo lavoro CK!
@Andrea, $BLUE a queste cifre non è regalata, ma torna interessante. Sicuramente le aspettative erano eccessive, probabilmente lo è stata anche la reazione ad ASH… fatico però a mettere dei punti fissi perché il focus ora è su indicazioni lontane da quelle di cui mi occupo abitualmente. Riguardo alla foto, come già detto, sono troppe le donne che si sono iscritte di recente alla newsletter per non tenerne conto nella scelta delle immagini… inoltre è giusto tributare i nerd in ogni occasione possibile.
@Juan, io fisserei però un punto sotto il quale non farle scendere…
GRAZIE MILLE C.K.
BACI
grazie CK!!! allora su TGTX tengo duro e aspetto news…ps gran bella foto 🙂 ..ONTX l ho mediata ieri sera mi fa piacere leggere che anche tu pensi ad un incremento della pos!! tuo sempre grato juan 🙂
Aspettavo 2 parole anche su Bluebird… Comunque ottimo lavoro come sempre … Ps mi aspettavo una foto più “spinta” ?